| 最新公告: |
|
2018年中国医药工业经济运行报告
2018年我国医药工业发展的主要经济指标继续保持稳定增长,研发投入加大、科技成果突出,质量体系进一步健全,国际化水平提升。但受国内宏观经济结构调整、医改进入深水区等叠加因素影响,也面临着不少困难与挑战。
一、2018年医药工业发展总体情况和运行特点
(一)整体收入和利润保持两位数增长
2018年,规模以上医药工业增加值同比增长9.7%,高于全国工业整体增速3.5个百分点。规模以上企业主营业务收入达到25840.0亿元,同比增长12.7%(注:对上年数作了调整),利润总额达到3364.5亿元,同比增长10.9%(注:对上年数作了调整),继续保持2017年以来两位数的增长速率。企业分化加剧,累计亏损企业数量达到14.3%,同比增长6.5%。各子行业中,主营业务收入增长最快的是化学药品制剂、卫生材料与医药用品以及生物药品制造,增速分别为19.4%、11.7%和11.4%;利润增长最快的是医疗仪器设备及器械、卫生材料与医药用品、中药饮片加工制造,增速分别为24.1%、16.7%和15.5%。
产业规模保持较快增长的主要原因:一是国内日益增长的健康需求促进购药金额的增加。2018年1-11月,全国医疗卫生机构总诊疗人次达75.4亿,同比提高3.3%。二是国家医保目录扩容,新增品种销售额实现快速增长。根据中国药学会2018年6月滚动
图1:2012~2018年医药工增加值增速与占比情况
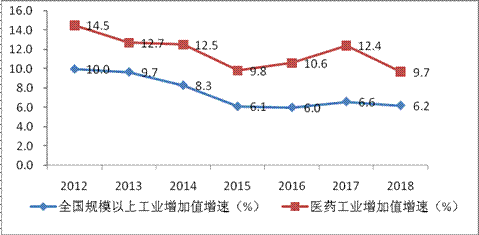
数据来源:国家统计局、工信部
图2:近6年医药工业主营业务收入增长情况
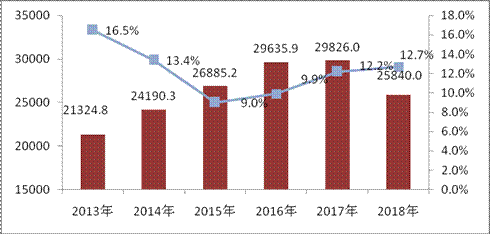
数据来源:工信部
图3:近6年医药工业利润增长情况
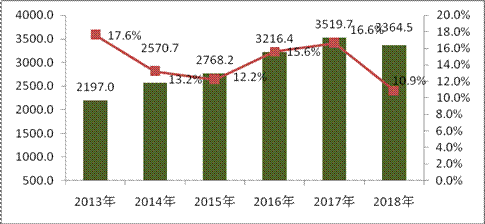
年数据,对比2009版及2017版医保目录品种使用情况,整体金额增幅达9.5%。2018年17种抗癌药通过价格谈判纳入医保,销售金额也实现快速增长。三是原料药涨价使部分品种国内销售和出口额增加。医药工业各子行业主营业务收入和利润总额如表1、表2。
表1 2018年医药工业各子行业主营业务收入
| 行业 | 主营业务收入(亿元) | 同比增长(%) | 比重(%) |
| 化学药品原料药制造 | 3843.3 | 10.4 | 14.9 |
| 化学药品制剂制造 | 8715.4 | 19.4 | 33.7 |
| 中药饮片加工 | 1714.9 | 11.2 | 6.6 |
| 中成药生产 | 4655.2 | 6.2 | 18.0 |
| 生物药品制造(含基因工程药物和疫苗制造) | 2443.0 | 11.4 | 9.5 |
| 卫生材料及医药用品制造(药物辅料及包装材料) | 1784.7 | 11.7 | 6.9 |
| 制药专用设备制造 | 161.3 | 9.9 | 0.6 |
| 医疗仪器设备及器械制造 | 2522.3 | 10.5 | 9.8 |
| 合计 | 25840.0 | 12.7 | 100.0 |
表2 2018年医药工业各子行业利润总额
| 行业 | 利润总额 (亿元) | 同比增长(%) | 比重(%) |
| 化学药品原料药制造 | 407.7 | 15.4 | 12.1 |
| 化学药品制剂制造 | 1195.0 | 8.7 | 35.5 |
| 中药饮片加工 | 139.1 | 15.5 | 4.1 |
| 中成药生产 | 641.0 | 3.8 | 19.1 |
| 生物药品制造 | 445.4 | 13.0 | 13.2 |
| 卫生材料及医药用品制造 | 182.7 | 16.7 | 5.4 |
| 制药专用设备制造 | 4.4 | -60.7 | 0.1 |
| 医疗仪器设备及器械制造 | 349.0 | 24.1 | 10.4 |
| 合计 | 3364.5 | 10.9 | 100.0 |
(二)创新环境持续改善,国产创新药进入收获阶段
获得多种来源支持,医药创新投入显著增加。一是企业研发投入增长。根据A股上市公司前三季度数据,287家医药上市公司研发投入合计223亿元,较上年同期明显增长,其中恒瑞医药、复星医药研发投入超过10亿元。二是资本市场积极投资创新药企业。2018年新药企业大额融资频现,多家企业融资超过10亿元;港交所允许未盈利的生物科技公司上市,年内已有5家国内生物科技企业获准上市,多家企业申报IPO。三是政府资金采取多种方式支持医药创新。重大新药创制专项等国家科技计划继续实施,国家和地方纷纷设立股权投资基金,医药产业是重点支持领域。四是新税收政策进一步引导医药企业加大研发投入。所有企业研发费用税前加计扣除比例提高到了75%,企业委托境外研发费用不得加计扣除的限制被取消。新药申报和获批大幅增长。全年国内企业共有230多个一类创新药申报注册 (包括申报临床和申报上市),10个一类新药获批上市,均为近年来新高。10个获批上市的一类新药中5个为抗肿瘤药物,3个为抗病毒药物,均围绕重大疾病治疗,针对未满足的临床需求。越来越多的具有自主知识产权的创新药获批上市,不仅有利于满足人民日益增长的健康需求,也促进了医药产业的转型升级。
(三)企业国际化步伐加快,医药出口向中高端迈进
2018年医药出口继续保持了较快增长,规模以上医药企业实现出口交货值2031.7亿元,同比增长11.5%,增速比上年同期提高0.4个百分点。拉动出口增长的仍主要是化学原料药,但整体
表3 2018年获批生产的国产一类创新药
| 序号 | 产品名称 | 生产厂家 | 适应症 |
| 1 | 盐酸安罗替尼胶囊 | 正大天晴 | 肿瘤 |
| 2 | 注射用艾博卫泰 | 前沿生物 | 艾滋病 |
| 3 | 马来酸吡咯替尼片 | 恒瑞医药 | 肿瘤 |
| 4 | 重组细胞因子基因衍生蛋白 | 杰华生物 | 乙肝 |
| 5 | 丹诺瑞韦钠片 | 歌礼药业 | 丙肝 |
| 6 | 呋喹替尼胶囊 | 和记黄埔 | 转移性结直肠癌 |
| 7 | 特瑞普利单抗注射液 | 君实生物 | 黑色素瘤 |
| 8 | 信迪利单抗注射液 | 信达生物 | 霍奇金淋巴瘤 |
| 9 | 硫培非格司亭注射液 | 恒瑞医药 | 粒细胞减少症 |
| 10 | 罗沙司他胶囊 | 珐博进 | 肾病贫血 |
表4 2018年申报上市的国产一类新药
| 序号 | 产品名称 | 生产厂家 | 适应症 | 申报时间 |
| 1 | 重组人乳头瘤病毒16/18型双价疫苗(大肠杆菌) | 厦门万泰沧海 | 宫颈癌等 | 2018年3月 |
| 2 | 重组人血管内皮抑素注射液 | 江苏吴中医药 | 肺癌 | 2018年3月 |
| 3 | 注射用卡瑞利珠单抗 | 苏州盛迪亚 | 霍奇金淋巴瘤 | 2018年4月 |
| 4 | 母牛分枝杆菌疫苗 | 安徽智飞 | 结核病 | 2018年5月 |
| 5 | 重组结核杆菌融合蛋白(EC) | 安徽智飞 | 结核菌感染鉴别等 | 2018年9月 |
| 6 | 替雷利珠单抗(PD-1) | 百济神州 | 霍奇金淋巴瘤 | 2018年9月 |
| 7 | 对甲苯磺酰胺注射液 | 天津红日药业 | 非小细胞肺癌 | 2018年1月 |
| 8 | 可利霉素片 | 上海同联制药 | 抗感染 | 2018年1月 |
| 9 | 优替德隆注射液 | 成都华昊中天 | 肿瘤 | 2018年3月 |
| 10 | 注射用甲苯磺酸瑞马唑仑 | 江苏恒瑞 | 麻醉 | 2018年3月 |
| 11 | 马来酸艾维替尼胶囊 | 浙江艾森药业 | 肺癌 | 2018年6月 |
| 12 | KW-136胶囊 | 北京凯因科技 | 丙肝 | 2018年6月 |
| 13 | 甲磺酸氟马替尼片 | 江苏豪森药业 | 白血病 | 2018年7月 |
| 14 | 赞布替尼胶囊 | 百济神州 | R/R套细胞淋巴瘤 | 2018年8月 |
| 15 | 盐酸拉维达韦片 | 歌礼药业 | 丙肝 | 2018年8月 |
| 16 | 注射用磷丙泊酚二钠 | 宜昌人福药业 | 麻醉 | 2018年10月 |
| 17 | 甘露寡糖二酸胶囊 | 上海绿谷 | 阿尔茨海默病 | 2018年11月 |
| 18 | 注射用苯磺酸瑞马唑仑 | 宜昌人福药业 | 麻醉 | 2018年11月 |
| 19 | 依达拉奉右旋莰醇注射液 | 南京先声 | 脑卒中 | 2018年11月 |
| 20 | 对甲苯磺酸尼拉帕利胶囊 | 再鼎医药 | 卵巢癌 | 2018年12月 |
| 21 | 盐酸恩莎替尼 | 贝达药业 | 非小细胞肺癌 | 2018年12月 |
出口结构逐步升级,重要标志是在欧美发达国家的药品注册不断增多。2018年共有23家企业的91个制剂品种获得美国ANDA批件(未含复星医药印度子公司),是2017年获批品种的2倍多,到2018年底,国内企业累计在美国注册的ANDA数量超过280个;共有6个制剂品种通过WHO预认证,到2018年底,累计25个制剂品种、50个原料药以及4个疫苗产品通过了该项认证。累计上百种新药在欧美发达经济体开展临床研究,除了一批大病用药外,有十几种新药拿到了约20项FDA孤儿药资格认定。
企业通过境外并购积极拓展国际市场。2018年医药行业多个境外并购项目超过5亿美元。在药品领域,企业通过并购获得产品和渠道,并购案例涉及抗肿瘤药、血液制品等多个方面。在医疗器械领域,并购金额创下了中资境外并购的新记录。
表5 2018年部分境外投资并购项目
| 序号 | 企业 | 金额 | 项目 |
| 1 | 华西股份与海辰药业 | 3.69亿 美元 | 收购意大利Nerviano Medical Sciences Group |
| 2 | 翰宇药业 | 1.2-1.8亿 欧元 | 收购德国AMWGmbH公司 |
| 3 | 哈药集团 | 3亿 美元 | 收购GNC公司 |
| 4 | 华东医药 | 约1.69亿英镑 | 收购英国Sinclair Pharma plc公司 |
| 5 | 上海莱士(天诚国际) | 9.4亿 欧元 | 收购德国BiotestAG公司 |
| 6 | 绿叶制药 | 5.46亿美元 | 收购阿斯利康旗下药物思瑞康 |
| 7 | 远大医药和鼎晖投资 | 14亿美元 | 收购澳洲肝癌治疗器械生产商Sirtex Medical |
| 8 | 蓝帆医疗 | 58.95亿元 | 收购新加坡柏盛国际公司 |
(四)企业生产质量水平稳步提升
国家药品监督管理局组织实施了一系列监管制度改革,并不断扩充职业化检查员队伍,在各个环节加大监管力度,促进了产品准入门槛提高,全生命周期的药品质量管理得到加强,部分落后产品逐步淘汰。一是仿制药一致性评价全面推进,仿制药质量水平系统提升。仿制药一致性评价成为多数化学药企业的中心任务,投入大量资源开展药品质量研究。截至2018年底,国家药品审评中心(CDE)共受理一致性评价申请708个,涉及253家企业的205个品种,已通过评价的申请共有149个,涉及76个品种(含视同通过)。二是药品研发与生产质量管理日益规范。随着国家药品监督环境的变化,企业质量责任更加明确,质量意识得到加强,质量体系不断健全,严格执行质量管理规范、努力提高产品质量成为多数企业的自发行为。三是药品质量标准逐步与国际接轨。2018年国家药品监督管理局成为国际人用药品注册技术协调会(ICH)的管理委员会成员,并积极推进ICH指导原则在中国的转化实施,对国内企业开展国际注册、提升药品质量体系具有重要意义。
二、影响医药行业发展的主要因素
(一)监管制度改革有力促进药物创新
从2015年国务院《关于改革药品医疗器械审评审批制度的意见》到2017年中办国办《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,文件中的相关要求逐步落实,为医药创新营造了良好的政策环境。2018年,药物临床试验审评正式采用60天默许制,大幅缩短药品审评周期;优先审评审批工作机制进一步优化,加快了药品的研发上市;上市许可持有人试点工作继续推进,调动了药品研发的积极性,有效减少了重复建设;原料药、药用辅料和药包材关联审评审批制度逐步实施,相关事宜更加明确;《关于改革完善仿制药供应保障及使用政策的意见》发布,将有力促进仿制药的研发与质量升级,加快仿制药替代原研品种。
(二)一致性评价政策推动仿制药结构调整
2016年以来,仿制药一致性评价持续推进,深刻影响仿制药格局。通过一致性评价的仿制药将获得多方面的政策鼓励,包括在招标采购中可与原研药同组竞争,加速替代原研;不能通过一致性评价的品种可能逐步退出市场,有利于仿制药质量整体提升和产业集中度提高。落实国务院《关于改革完善仿制药供应保障及使用政策的意见》,2018年已有20多个省份出台了相关鼓励政策,使通过一致性评价的品种快速实现销售,从而调动企业开展一致性评价的积极性。
(三)医保政策改革提高人民群众用药可及性
2018年,集中采购、医保谈判、医保统筹等多项医保政策的实施,有效提高了人民群众用药可及性。主要包括:开展抗癌药省级专项集中采购工作;下调14种前期国家谈判抗癌药的支付标准和采购价格;将17种抗癌药谈判品种纳入医保;推进城乡居民医疗保险整合,提高医保财政补助;逐步扩大按病种付费的病种数量等。2018年5月国家医疗保障局正式挂牌成立,集药品和医疗服务价格管理、药品集中招标、医保支付三项职能于一体,将在改革医保支付方式、制定医保支付标准、控制药品费用不合理增长、提高医保资金使用效率方面发挥重要作用,更好地保障人民群众的用药需求。
(四)医药流通格局加快重塑
随着药品生产流通政策调整与“互联网+医疗健康”的发展,医药流通格局加快重塑。一是“两票制”在全国范围内全面推开,医药流通行业加速整合,拥有品种资源和渠道优势的全国性医药流通企业扩大份额,而一批中小型医药流通公司逐渐退出市场。二是医药电子商务成为重要的发展模式,B2B、B2C、O2O等多元化的医药电子商务迅速发展,除阿里等医药电商平台外,流通企业、零售连锁药店也纷纷涉足电商领域。三是医药零售市场集中度及零售连锁率不断提高,业外资本、医药和零售连锁企业积极参与零售药店的并购整合,加速了医药零售行业的格局变化。
(五)控费背景下需求侧拉动行业增长动力弱化
医药市场受到健康需求促进和控费抑制两方面因素的影响,近年来医保和医疗机构控费力度不断加大,健康需求对行业增长的拉动作用被弱化。控费政策主要包括公立医院医疗费用增幅控制、降低药占比以及各种形式降低药价等。2018年医疗机构控费仍是医改的重点,从抗癌药谈判降价、“4+7”城市带量采购试点、DRGs付费试点以及拟制定全国辅助用药目录,都对医药终端需求增长产生了一定制约影响。若《国家组织药品集中采购试点方案》扩大实施,将对医药市场今后发展带来巨大影响。
(六)原料药产业面临环保压力
化学原料药处于医药产业链的上游,是保障下游制剂生产、满足临床用药需求的基础。由于近年来,受环保政策影响,原料药产业面临多重压力。我国原料药生产厂家众多,很多中小企业生产粗放,绿色生产水平低,无法实现三废达标排放。随着近年国家不断加强环保监管,特别是新《环境保护法》实施,水污染防治行动计划、大气污染防治行动计划深入推进,实施《打赢蓝天保卫战三年行动计划》,很多企业被限产或停产,导致原料药供求关系变化,出现很多品种价格上涨,不利于产品稳定供应和行业可持续发展。
三、2019年医药工业发展展望
(一)主营业务收入保持稳定增长
尽管面临医院控费、药品降价等诸多不利影响,但2019年医药工业发展也有很多有利因素。主要包括:居民健康消费结构升级,新药上市增多以及医保目录新增品种放量,医保收入稳定增长、省级统筹增多及城乡居民医保整合,原料药价格稳定并有利出口,《2018—2020年大型医用设备配置规划》出台,新增采购量可观等。预计2019年医药工业主营业务收入仍将保持稳定增长,但增速可能会出现下降。
(二)医药创新继续保持良好态势
药品审评审批制度改革、临床试验默许制、药品专利保护、创新药纳入医保、药品上市许可持有人制度等政策的深入推进,以及资本市场对创新药的支持,将持续激发企业的创新活力。2018年一批国产创新药提交上市申请,预计2019年新产品上市数量将多于2018年。此外,随着仿制药价格进一步下降,以及医保政策向创新药倾斜,一些企业逐渐将发展重点转向创新药,研发投入将继续加大。
(三)带量采购改变仿制药发展格局
随着通过一致性评价的仿制药品种增加,带量采购涉及的药品范围可能进一步扩大。带量采购品种以仿制药一致性评价为门槛,将倒逼部分仿制药企业退出,加速原研药的国产替代,加剧产品价格竞争。仿制药盈利模式将逐步和国外趋同,产品进入低毛利、低费用发展阶段,仿制药企业未来会向高效率、低成本、规模化、制剂差异化、仿创结合的方向发展。
(四)国际化发展进一步升级
随着国内企业研发能力提高,以及国家政策鼓励,2019年在境外开展临床试验的创新药将继续增加,更多的产品进入三期临床研究阶段。绿叶制药的注射用利培酮缓释微球已获得美国食品药品监督管理局的NDA申请号,进入上市申报准备的最后阶段,有望于2019年在美国上市。国内企业已经开始由大宗原料药和普通制剂出口,向新药原料药CDMO、高端制剂、创新药等更高层次的国际化方向延申,国际化发展逐步升级。
(五)生物药产业进入快速发展阶段
近年来我国以抗体药物、重组蛋白质药物和疫苗为代表的生物药发展迅速,紧跟国际先进技术步伐,涌现出了一批优秀的企业和产品。以抗体药物为例,有300多家企业在从事研发或生产,一批新药和生物类似药进入临床,涵盖了几乎所有全球销售领先的靶点,2018年有两款PD-1抑制剂获批上市,将为提高国内患者用药水平发挥重要作用。随着国家政策支持、大批在研项目推进以及专业化CRO/CMO机构支撑,预计2019年生物药的申报和获批将迎来一个高峰期。
四、促进产业发展的相关政策建议
一是规划引导产业健康发展。围绕《医药工业发展规划指南》确定的重点发展领域和支持方向,以创新驱动和绿色发展为指引,推进医药制造业创新中心建设,推动化学原料药绿色发展,提升医药领域智能发展水平,实现医药工业高质量发展。
二是协同加大财税金融支持。在整体降税减负政策导向下,协调相关部门落实医药产业发展的更多税收优惠政策。推动提高药品制剂出口退税率,拓宽医药企业融资渠道,鼓励金融机构支持早期医药项目和创新型中小企业发展,建立健全创新成果商业转化机制。
三是协调完善药物使用政策。跟踪分析国家药品集中采购试点政策对行业发展的影响,配合相关部门不断完善优化。推动新上市药品尽快纳入医疗机构诊疗指南和临床路径,促进新产品合理应用。推行患者凭医院处方到零售药店自主购买慢病常见病用药,并纳入医保报销范围,增强社会药房服务能力。
四是积极培育新型增长点。推动加快具有较大临床价值药品审批上市,鼓励疗效确切、临床必需的新产品扩大应用。积极发展医药产业新模式、新业态,促进行业转型升级和提质增效。巩固原料药出口优势,重点拓展发达国家和新兴医药市场,提高制剂出口规模和产品附加值。
五是完善多层次医疗保障体系。推动医保支付方式改革,建立统一的医保支付标准,促进通过一致性评价仿制药优先使用。鼓励发展商业健康保险,支持商业保险产品创新,扩大商业健康保险个人所得税优惠幅度,引导提升公众保险意识和消费认知,逐步提高医疗保障水平。
文稿提供:中国医药企业管理协会

 京公网安备 11040102700142号
京公网安备 11040102700142号